طبيعة وأصل الفيروسات. أضرار وفوائد الفيروسات
تلعب الفيروسات دورًا مهمًا في حياة الإنسان، حيث يمكن أن تسبب أمراضًا متفاوتة الخطورة.
حسب الخصائص الوبائية تنقسم الأمراض الفيروسية إلى بشري إذنهناك تلك التي تؤثر على البشر فقط (على سبيل المثال، شلل الأطفال) و حيواني -التي تنتقل من الحيوانات إلى الإنسان (على سبيل المثال، داء الكلب).
الطرق الرئيسية لانتقال العدوى الفيروسية هي:
1. طريق الطعام، حيث يدخل الفيروس إلى جسم الإنسان عن طريق الطعام والماء الملوثين (التهاب الكبد الفيروسي A، E، وما إلى ذلك)
2. بالحقن (أو عن طريق الدم) فيها فايروسيدخل مباشرة إلى الدم أو البيئة الداخلية للشخص. ويحدث هذا بشكل رئيسي عند التعامل مع الأدوات الجراحية أو المحاقن الملوثة، أثناء الاتصال الجنسي غير المحمي، وكذلك عبر المشيمة من الأم إلى الطفل. تنتقل بهذه الطريقة الفيروسات الهشة التي تتحلل بسرعة في البيئة (فيروس التهاب الكبد B، فيروس نقص المناعة البشرية، فيروس داء الكلب، إلخ).
3. الجهاز التنفسيوالذي يتميز بآلية انتقال محمولة جوا، حيث يدخل الفيروس إلى جسم الإنسان مع الهواء المستنشق، الذي يحتوي على جزيئات من البلغم والمخاط التي يخرجها شخص مريض أو حيوان. وهذا هو أخطر طرق انتقال العدوى، حيث يمكن أن ينتقل الفيروس عبر الهواء لمسافات كبيرة ويسبب أوبئة كاملة. هذه هي الطريقة التي تنتقل بها فيروسات الأنفلونزا ونظير الأنفلونزا والنكاف وجدري الماء وما إلى ذلك.
معظم الفيروسات لديها تقارب معين لهذا العضو أو ذاك. على سبيل المثال، تتكاثر فيروسات التهاب الكبد في المقام الأول في خلايا الكبد. حسب نوع الأعضاء المستهدفة التي تتأثر أثناء مرض معين، نميز الأنواع التالية من الأمراض الفيروسية: المعوية، التنفسية (الجهاز التنفسي)، التي تؤثر على الجهاز العصبي المركزي والمحيطي، الأعضاء الداخلية، الجلد والأغشية المخاطية، الأوعية الدموية، الجهاز المناعي. ، إلخ. حسب النوع نتميز بالتطور السريري الالتهابات الفيروسية الحادة والمزمنة.الاكثر انتشارا الأمراض الفيروسية الحادة،والتي تحدث مع أعراض محلية واضحة (تلف الغشاء المخاطي للجهاز التنفسي، تلف أنسجة الكبد، تلف مناطق مختلفة من الدماغ) والطابع العام - زيادة درجة حرارة الجسم، والضعف، وآلام في المفاصل والعضلات، والتغيرات في تكوين الدم، وما إلى ذلك. عدوى فيروسية حادة، مثل عادة ما تنتهي بالشفاء التام للجسم. وفي بعض الحالات، يصبح الشكل الحاد للمرض مزمنا. مزمنتحدث الالتهابات الفيروسية بصورة سريرية غير واضحة وفي بعض الأحيان قد لا يلاحظها المرضى أنفسهم. يصعب علاج الالتهابات المزمنة ويمكن أن تستمر لفترة طويلة، مما يؤدي إلى تغيرات شكلية ووظيفية كبيرة في الأعضاء الداخلية (على سبيل المثال، يمكن أن يؤدي التهاب الكبد المزمن B إلى تليف الكبد).
وبطبيعة الحال، لا يمكن مقارنة الأشكال الحديثة من الفيروسات بالأشكال الأولية للحياة. ويجب أن تختلف عن الأخيرة نتيجة للتطور التاريخي الذي مرت به، ولكنها تحتفظ بالسمات النموذجية العامة للتنظيم غير الخلوي.
مع اكتشاف الفيروسات في عام 1892 من قبل D. I. تم ملء إيفانوفسكي الفجوة في تاريخ تطور الكائنات الحية. إن موقف إنجلز حول فترة طويلة من التطور التاريخي للكائنات غير الخلوية قد تجسد في عالم الفيروسات.
طبيعة الفيروسات.تحتل الفيروسات مكانة خاصة مقارنة بمجموعات الكائنات الحية الدقيقة الأخرى. إنهم كما لو كانوا على الحدود بين الطبيعة الحية وغير الحية. وكانت طبيعتها موضوع العديد من الدراسات والمناقشات عبر تاريخ علم الفيروسات. ما هي - كائنات أو مواد، كائن له خصائص المادة أو العكس؟ وطرح هذه الأسئلة يدل على الطبيعة المزدوجة لخصائصها. في الواقع، في البيئة الخارجية، تعد الفيروسات، بما في ذلك العاثيات، تكوينات خاملة تمامًا ولا تظهر عليها علامات الحياة - التنفس والتغذية والتكاثر. يمكن تحويل الكثير منهم إلى بلورات. في حالة بلورية أو مجففة، يمكن الحفاظ عليها لسنوات عديدة. أنها تتصرف مثل المركبات الكيميائية. ولكن بمجرد دخولهم إلى الخلايا الحساسة، تبدأ جميع علامات الحياة في الظهور فيها - التكاثر، والوراثة، والتقلب، والقدرة على التكيف، والتطور.
يعتبر عالم الفيروسات الأمريكي البارز دبليو إم ستانلي أن ازدواجية طبيعتها هي سمة مميزة للفيروسات. في حالته الحرة، يكون الفيروس ببساطة جزيءًا عملاقًا يتمتع بجميع الميزات الكامنة في جميع الجزيئات الكبيرة. في الخلية الحية، يتجلى ككائن حي، ويتكاثر ويتحور. وبالتالي، فإن TMV إما أن يكون أصغر كائن حي أو أكبر جزيء.
بعض العلماء، بناءً على قدرة الفيروسات على التبلور والإنزيمات على التحفيز الذاتي، أي التحفيز تحت تأثير المنتجات المنطلقة نتيجة التفاعل نفسه، يصنفون الفيروسات على أنها إنزيمات. لكن التركيب الكيميائي للفيروسات والإنزيمات يرفض طبيعتها الأنزيمية. الإنزيمات هي مواد بروتينية، والفيروسات، بالإضافة إلى البروتينات، تحتوي أيضًا على أحماض نووية توجه تركيب البروتينات. تعتمد ظاهرة التبلور على كتلة وبنية الجزيئات التي تشكل الشبكة البلورية. إن كتلة البكتيريا والريكتسيا والفيروسات الكبيرة كبيرة جدًا بحيث لا يمكنها أن تصبح وحدات هيكلية من البلورات. يمكن للفيروسات الصغيرة الحجم أن تتبلور بسبب عمل قوى الالتصاق بين الجزيئات والبنية الفيزيائية والكيميائية للجزيئات.
إن الجدل الدائر حول طبيعة الفيروسات ليس ذا أهمية نظرية فحسب، بل له أهمية عملية كبيرة أيضًا. ومن الواضح أن إجراءات مكافحة الأمراض الفيروسية التي تصيب الإنسان والحيوان والنبات ستكون مختلفة تماماً اعتماداً على ما إذا كانت ناجمة عن كائنات حية، أو أنها تنشأ نتيجة دخولها إلى الجسم أو تكون بعض المواد فيه. . تعتمد جميع تدابير مكافحة الالتهابات الفيروسية على التعرف على الطبيعة الحية للفيروسات. وقد أثبتت الممارسة فعالية هذه التدابير.
تطورت الأفكار الحديثة حول الفيروسات تدريجياً. في عام 1892 دي. لفت إيفانوفسكي الانتباه إلى مرض التبغ واسع الانتشار، حيث تكون الأوراق مغطاة ببقع متناثرة (مرض الفسيفساء). بعد اكتشاف إيفانوفسكي للفيروسات، تم اعتبارها مجرد كائنات دقيقة صغيرة جدًا، غير قادرة على النمو على الوسائط المغذية الاصطناعية. بعد وقت قصير من اكتشاف فيروس فسيفساء التبغ، تم إثبات الطبيعة الفيروسية لمرض الحمى القلاعية، وبعد سنوات قليلة تم اكتشاف العاثيات. وهكذا تم اكتشاف ثلاث مجموعات رئيسية من الفيروسات التي تصيب النباتات والحيوانات والبكتيريا. ومع ذلك، لفترة طويلة، تطورت هذه الفروع المستقلة لعلم الفيروسات بمعزل عن غيرها، وكانت الفيروسات الأكثر تعقيدًا - العاثيات - لفترة طويلة لا تعتبر مادة حية، بل شيئًا مثل الإنزيمات. ومع ذلك، بحلول نهاية العشرينيات وبداية الثلاثينيات، أصبح من الواضح أن الفيروسات هي مادة حية، وفي نفس الوقت تقريبًا تم تخصيص أسماء الفيروسات القابلة للتصفية أو الفيروسات الفائقة لها.
في أواخر الثلاثينيات وأوائل الأربعينيات، تقدمت دراسة الفيروسات كثيرًا لدرجة أن الشكوك حول طبيعتها الحية اختفت، وتم صياغة مفهوم الفيروسات ككائنات حية. أساس الاعتراف بالفيروسات ككائنات هو الحقائق التي تم الحصول عليها أثناء دراستها، والتي تشير إلى أن الفيروسات، مثل الكائنات الحية الأخرى (الحيوانات والنباتات والأوالي والفطريات والبكتيريا)، قادرة على التكاثر، ولها الوراثة والتنوع، والقدرة على التكيف مع البيئة. الظروف المتغيرة لبيئتهم، وأخيرا، القابلية للتطور البيولوجي، الناجم عن الانتقاء الطبيعي أو الاصطناعي. هذا هو في المقام الأول تفاعل اثنين من الجينوم - الفيروسي والخلوي.
ووفقا للثالث، فإن الفيروسات هي مشتقات من الهياكل الجينية الخلوية التي أصبحت مستقلة نسبيا، ولكنها تحتفظ باعتمادها على الخلايا. بدت الفرضية الثالثة التي تتراوح ما بين 20 إلى 30 عامًا غير محتملة، بل إنها تلقت الاسم الساخر لفرضية الجينات المجنونة. ومع ذلك، فإن الحقائق المتراكمة توفر المزيد والمزيد من الحجج الجديدة لصالح هذه الفرضية. إلى جانب ذلك، تراكم عدد كبير من الحقائق التي تشير إلى وجود تبادل واسع النطاق في الطبيعة لكتل المعلومات الجينية الجاهزة، بما في ذلك بين ممثلي الفيروسات المختلفة البعيدة تطوريًا. ونتيجة لهذا التبادل، يمكن أن تتغير الخصائص الوراثية بسرعة وبشكل مفاجئ من خلال دمج الجينات الأجنبية (استعارة وظيفة الجينات). يمكن أيضًا أن تنشأ صفات وراثية جديدة بسبب مزيج غير متوقع من الجينات الخاصة والمتكاملة (ظهور وظيفة جديدة). وأخيرًا، فإن الزيادة البسيطة في الجينوم بسبب الجينات غير العاملة تفتح إمكانية تطور هذه الأخيرة (تكوين جينات جديدة).
ما هي أشكال الحياة غير الخلوية؟
يعض بشكل مؤلم وهجومي ،
رغم أنك لا تستطيع رؤيته في بعض الأحيان..
جي سويفت
"حسنًا، دع غريبتنا الجميلة تبقى غريبة، طالما أنها تحبنا"؟ قال، وفقا للأسطورة، عالم الأحياء الدقيقة المتميز L. باستور، بعد أن فشل في عزل العامل المسبب لداء الكلب؟ مرض رهيب لم يكن هناك خلاص منه في القرن التاسع عشر. لقد تمكن من الحصول على لقاح وبالتالي فهم طبيعة العامل المعدي وإنقاذ عدة آلاف من الأرواح البشرية. لم يكن من الممكن لأحد أن يفعل ذلك في تلك الأيام، لأن العامل المسبب لداء الكلب لم يكن ميكروبًا، كما توقع إل. باستور، بل كان فيروسًا.
جنبا إلى جنب مع الكائنات وحيدة الخلية ومتعددة الخلايا، هناك أشكال أخرى من الحياة في الطبيعة. هذه فيروسات ليس لها بنية خلوية. إنها تمثل شكلاً انتقاليًا بين المادة الحية وغير الحية. الفيروسات بسيطة للغاية. يتكون كل جسيم فيروسي من الحمض النووي الريبوزي (RNA) أو الحمض النووي (DNA) المحاط بغلاف بروتيني يسمى قفيصة,يسمى الجسيم المعدي المكتمل فيريون. بعض الفيروسات (الهربس أو الأنفلونزا) لها أيضًا غلاف إضافي ينشأ من الغشاء البلازمي للخلية المضيفة. يمكن للفيروسات أن تعيش وتتكاثر فقط في خلايا الكائنات الحية الأخرى. وفي البيئة الخارجية لا تظهر عليها أي علامات للحياة، والعديد منها على شكل بلورات. ويتراوح حجم الفيروسات من 20 إلى 300 نانومتر.
يحتوي الفيروس على بنية داخلية معقدة إلى حد ما. يحتوي جوهرها (جوهرها) على جزيء حمض نووي واحد (أحيانًا أكثر) (DNA أو RNA). تحتوي الأحماض النووية لأصغر الفيروسات على 3-4 جينات، بينما تحتوي أكبر الفيروسات على ما يصل إلى 100 جين. ومن الخارج، يتم تغطية الفيروس بـ "غطاء" بروتيني يحمي الحمض النووي من التأثيرات البيئية الضارة. شكل الفيروسات متنوع للغاية. بناءً على حجمها، تنقسم الفيروسات إلى كبيرة (قطرها 300-400 نانومتر)، ومتوسطة (80-125 نانومتر)، وصغيرة (20-30 نانومتر). يمكن رؤية الفيروسات الكبيرة بالمجهر العادي، بينما تتم دراسة الفيروسات الصغيرة تحت المجهر الإلكتروني.
الجامعة: جامعة ولاية جنوب الأورال
السنة والمدينة: تشيليابينسك 2011
مقدمة 4
خواص الفيروسات. طبيعة الفيروسات 5
II هيكل وتصنيف الفيروسات 7
III تفاعل الفيروس مع الخلية 10
رابعا معنى الفيروسات 12
V بعض أشهر الأمراض الفيروسية البشرية 15
سادسا هل الفيروسات حية؟ 17
السابع على قيد الحياة إلى الأبد 19
الاستنتاج.22
القائمة الببليوغرافية.23
حاشية. ملاحظة
فيدوروفا أ.ف. "الفيروسات هي شكل انتقالي من عدم العيش إلى العيش." - تشيليابينسك: جامعة جنوب الأورال الحكومية، EiP - 114، 2011، 23 ص، 11 مريض، جدول واحد، ببليوجر. القائمة - 9 عناصر.
يناقش هذا الملخص قضايا مثل خصائص وطبيعة الفيروسات. بعض خصائص الفيروسات هي: أنها تحتوي على نوع واحد فقط من الأحماض النووية، وليس لها عملية التمثيل الغذائي الخاصة بها، وما إلى ذلك. البنية والتصنيف، تفاعل الفيروس مع الخلية (الفيروسات قادرة على العيش والتكاثر فقط في خلايا الكائنات الحية الأخرى. ولا تظهر أي علامات على الحياة خارج خلايا الكائنات الحية). أهمية الفيروسات، بعض الأمراض الفيروسية (الحصبة، النكاف، الأنفلونزا، شلل الأطفال، داء الكلب، الجدري، الحمى الصفراء، التراخوما، التهاب الدماغ، بعض أمراض الأورام (الورم)، الإيدز). يتم طرح السؤال "هل الفيروسات حية؟"
مقدمة
وبحلول نهاية القرن الماضي، لم يكن أحد يشك في أن كل مرض معد يسببه ميكروب خاص به، ويمكن مكافحته بنجاح.
قال علماء البكتيريا: «فقط أعطهم الوقت، وقريبًا لن يكون هناك مرض واحد». لكن مرت السنوات ولم يتم الوفاء بالوعود. أصيب الناس بالحصبة ومرض الحمى القلاعية وشلل الأطفال والتراخوما والجدري والحمى الصفراء والأنفلونزا. مات الملايين من الناس من أمراض رهيبة، ولكن لم يتم العثور على الميكروبات التي تسبب لهم.
وأخيرا في عام 1892 العالم الروسي د. كان إيفانوفسكي على الطريق الصحيح. أثناء دراسته لفسيفساء التبغ، وهو مرض يصيب أوراق التبغ، توصل إلى استنتاج مفاده أن المرض لم يكن بسبب ميكروب، بل بسبب شيء أصغر. يخترق هذا "الشيء" أدق المرشحات القادرة على الاحتفاظ بالبكتيريا، ولا يتكاثر في الوسائط الاصطناعية، ويموت عند تسخينه، ولا يمكن رؤيته بالمجهر الضوئي. سم قابل للتصفية!
وكان هذا استنتاج العالم. لكن السم مادة، والعامل المسبب لمرض التبغ هو مخلوق. تتكاثر بشكل جيد في أوراق النبات. أطلق عالم النبات الدنماركي مارتن ويليم بيرينيك على هذا "الشيء" الجديد اسم فيروس، مضيفًا أن الفيروس هو "شيء سائل وحي ومعدي". ترجمت كلمة "فيروس" من اللغة اللاتينية وتعني "السم".
وبعد بضع سنوات، اكتشف F. Leffler وP.Frosch أن العامل المسبب لمرض الحمى القلاعية، وهو مرض يوجد غالبًا في الماشية، يمر أيضًا عبر المرشحات البكتيرية. أخيرًا، في عام 1917، اكتشف عالم البكتيريا الكندي ف. دي هيريل البكتيريا - وهو فيروس يصيب البكتيريا.
وهكذا تم اكتشاف فيروسات النباتات والحيوانات والكائنات الحية الدقيقة. كانت هذه الأحداث بمثابة بداية لعلم جديد - علم الفيروسات، دراسة أشكال الحياة غير الخلوية.
خصائص الفيروسات. طبيعة الفيروسات
2) ليس لديها عملية التمثيل الغذائي الخاصة بها ولديها عدد محدود للغاية من الإنزيمات. للتكاثر، يتم استخدام عملية التمثيل الغذائي للخلية المضيفة وإنزيماتها وطاقتها؛
لا تتكاثر الفيروسات على الوسائط المغذية الاصطناعية - فهي انتقائية للغاية فيما يتعلق بالطعام. مرق اللحم العادي الذي يناسب معظم أنواع البكتيريا غير مناسب للفيروسات . إنهم بحاجة إلى خلايا حية، وليس فقط أية خلايا، بل إلى خلايا محددة بدقة. مثل الكائنات الحية الأخرى، الفيروسات قادرة على التكاثر. الفيروسات وراثية . يمكن أن تؤخذ الخصائص الوراثية للفيروسات في الاعتبار من خلال نطاق العوائل المصابة وأعراض الأمراض المسببة، بالإضافة إلى خصوصية الاستجابات المناعية للعوائل الطبيعية أو حيوانات التجارب المحصنة صناعيًا. إن مجموع هذه الخصائص يجعل من الممكن تحديد الخصائص الوراثية لأي فيروس بوضوح، بل وأكثر من ذلك - أصنافه التي لها علامات وراثية واضحة، على سبيل المثال: التوجه العصبي لبعض فيروسات الأنفلونزا، وما إلى ذلك. . التباين هو الوجه الآخر للوراثة، وفي هذا الصدد تشبه الفيروسات جميع الكائنات الحية الأخرى التي تعيش على كوكبنا. في الوقت نفسه، في الفيروسات، من الممكن ملاحظة التباين الوراثي المرتبط بالتغيرات في المادة الوراثية، والتقلب المظهري المرتبط بمظهر نفس النمط الوراثي في ظروف مختلفة.
II هيكل وتصنيف الفيروسات
لا يمكن رؤية الفيروسات بالمجهر الضوئي لأن أحجامها أصغر من الطول الموجي للضوء. ولا يمكن رؤيتها إلا باستخدام المجهر الإلكتروني.
تتكون الفيروسات من المكونات الرئيسية التالية.
1. المادة الوراثية الأساسية (DNA أو RNA)، التي تحمل معلومات حول عدة أنواع من البروتينات اللازمة لتكوين فيروس جديد؛
2. القشرة البروتينية والتي تسمى القفيصة (من الكلمة اللاتينية capsa - box). غالبًا ما يتم بناؤه من وحدات فرعية متكررة متطابقة - القسيمات القسيمية. تشكل القسيمات القفيصية هياكل ذات درجة عالية من التماثل؛
3. غشاء البروتين الدهني الإضافي. يتكون من الغشاء البلازمي للخلية المضيفة ويوجد فقط في الفيروسات الكبيرة نسبيًا (الأنفلونزا والهربس).
تتمتع الكبسولات والقشرة الإضافية بوظائف وقائية، كما لو كانت تحمي الحمض النووي. بالإضافة إلى أنها تسهل دخول الفيروس إلى الخلية. يسمى الفيروس المكتمل التكوين virion.
يظهر الهيكل التخطيطي لفيروس يحتوي على الحمض النووي الريبي (RNA) مع نوع حلزوني من التناظر ومغلف إضافي من البروتين الدهني على اليسار في الشكل 1؛ ويظهر مقطع عرضي موسع على اليمين.
الشكل 1. الهيكل التخطيطي للفيروس: 1 - النواة (RNA المفرد)؛ 2 - غلاف البروتين (قفيصة)؛ 3 - غشاء البروتين الدهني الإضافي. 4 - القفيصيات (الأجزاء الهيكلية للقفيصة)
إن عدد القسيمات القسيمية وطريقة طيها ثابت تمامًا لكل نوع من الفيروسات. على سبيل المثال، يحتوي فيروس شلل الأطفال على 32 قسيمة قسيمية، ويحتوي الفيروس الغدي على 252 قسيمة.
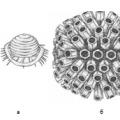
وبما أن أساس كل الكائنات الحية هو الهياكل الجينية، فقد تم تصنيف الفيروسات الآن وفقا لخصائص مادتها الوراثية - الأحماض النووية. تنقسم جميع الفيروسات إلى مجموعتين كبيرتين : فيروسات الحمض النووي(فيروسات ديوكسي) و فيروسات الحمض النووي الريبي(الفيروسات الريبو). يتم بعد ذلك تقسيم كل مجموعة من هذه المجموعات إلى فيروسات حمض نووي مزدوجة السلسلة وفيروسات أحادية السلسلة. المعيار التالي هو نوع التماثل للفيريونات (اعتمادًا على طريقة وضع القسيمات)، ووجود أو عدم وجود أصداف خارجية، وفقًا للخلايا - المضيف. وبالإضافة إلى هذه التصنيفات، هناك العديد من التصنيفات الأخرى. على سبيل المثال، حسب نوع انتقال العدوى من كائن حي إلى آخر.

الشكل 2. تمثيل تخطيطي لترتيب القسيمات القفيصية في القفيصة الفيروسية. يحتوي فيروس الأنفلونزا على نوع حلزوني من التماثل. نوع التماثل المكعب في الفيروسات: الهربس - ب، الفيروس الغدي - ج، شلل الأطفال - د
صدَفَة.
الفيروسات المغلفة، على عكس الخلايا الطبيعية، لا تملك القدرة على إصلاح الأغشية الدهنية التالفة. يمكن للنظام المكمل الاستفادة من هذا الضعف، لأن أدنى ضرر للغشاء الخارجي سيؤدي إلى تمزقه، وبالتالي فقدان الخصائص المعدية للفيروس. ومن الواضح أن النظام المكمل، وهو جزء من جهاز المناعة الفطري، يلعب دورا حاسما في مكافحة الالتهابات الفيروسية. ومع ذلك، يمكن أن تكون MPC فعالة فقط ضد مسببات الأمراض التي لها غشاء دهني خارجي. البكتيريا إيجابية الجرام أو الخميرة، التي لها جدار خلوي إضافي، غير معرضة للتكميل.
الشكل 3- بنية الحمض النووي للفيروسات
أ) فيروسات الجدري
ب) الهربس - الفيروسات
الحمض النووي الريبي المفرد الذين تقطعت بهم السبل
ج) فيروسات الحصبة والنكاف
د) فيروسات داء الكلب
ه) فيروسات اللوكيميا والإيدز
بدون صدفة
الحمض النووي المزدوج تقطعت بهم السبل
ه) القزحية - الفيروسات
ز) الغدية - الفيروسات
III تفاعل الفيروس مع الخلية
يمكن للفيروسات أن تعيش وتتكاثر فقط في خلايا الكائنات الحية الأخرى. أما خارج خلايا الكائنات الحية فلا تظهر عليها أية علامات للحياة. في هذا الصدد، تكون الفيروسات إما شكلًا ساكنًا خارج الخلية (فاريون) أو شكلًا متكاثرًا داخل الخلايا - نباتيًا. تظهر الاختلافات جدوى ممتازة. على وجه الخصوص، يمكنهم تحمل ضغوط تصل إلى 6000 ضغط جوي. وتتحمل جرعات عالية من الإشعاع، ولكنها تموت عند درجات الحرارة المرتفعة، والتعرض للأشعة فوق البنفسجية، وكذلك التعرض للأحماض والمطهرات.
يمر تفاعل الفيروس مع الخلية بعدة مراحل بالتتابع.
1. المرحلة الأولى هي امتصاص المتغيراتعلى سطح الخلية المستهدفة، والتي لهذا الغرض يجب أن تحتوي على المستقبلات السطحية المناسبة. معهم يتفاعل الجسيم الفيروسي على وجه التحديد، وبعد ذلك يتم ربطه بقوة، ولهذا السبب، فإن الخلايا ليست عرضة لجميع الفيروسات. وهذا ما يفسر التحديد الصارم لطرق اختراق الفيروسات. على سبيل المثال، تحتوي الخلايا الموجودة في الغشاء المخاطي للجهاز التنفسي على مستقبلات لفيروس الأنفلونزا، لكن خلايا الجلد لا تفعل ذلك. لذلك، لا يمكن أن تنتقل الأنفلونزا عبر الجلد - يجب استنشاق الجزيئات الفيروسية بالهواء، ويخترق فيروس التهاب الكبد A أو B ويتكاثر فقط في خلايا الكبد، وفيروس النكاف (النكاف) - في خلايا الغدد اللعابية النكفية. ، إلخ.
2. المرحلة الثانية تتكون من اختراقكامل الفاريون أو حمضه النووي إلى الخلية المضيفة.
3. المرحلة الثالثة تسمى إزالة البروتين. خلال هذه العملية، يتم إطلاق المادة الحاملة للمعلومات الجينية للفيروس، وهو حمضه النووي.
4. خلال المرحلة الرابعة، والتي تعتمد على الحمض النووي الفيروسي، تخليق المركبات اللازمة للفيروس.
5. في المرحلة الخامسة يحدث توليف مكونات الجسيمات الفيروسية- الحمض النووي والبروتينات القفيصة، ويتم تصنيع جميع المكونات عدة مرات.
6. خلال المرحلة السادسة، تم تصنيع نسخ عديدة من الحمض النووي والبروتينات مسبقًا تتشكل الفيروسات الجديدة عن طريق التجميع الذاتي
7. المرحلة الأخيرة - السابعة - تمثل إطلاق الجزيئات الفيروسية المجمعة حديثًا من الخلية المضيفة. تحدث هذه العملية بشكل مختلف بالنسبة للفيروسات المختلفة. في بعض الفيروسات، يكون هذا مصحوبًا بموت الخلايا بسبب إطلاق الإنزيمات المحللة في الليزوزومات. تحلل الخلية.وفي حالات أخرى، تترك المتغيرات الخلية الحية عن طريق التبرعم، ولكن حتى في هذه الحالة تموت الخلية بمرور الوقت.
رابعا أهمية الفيروسات
يعرف العلم فيروسات البكتيريا والنباتات والحشرات والحيوانات والبشر. يوجد أكثر من 1000 منها، ويؤدي تكاثر الفيروسات المرتبطة بتدمير الخلايا إلى حدوث حالات مؤلمة في الجسم. تسبب الفيروسات العديد من الأمراض للإنسان: الحصبة والنكاف والأنفلونزا وشلل الأطفال وداء الكلب والجدري والحمى الصفراء والتراخوما والتهاب الدماغ وبعض أمراض الأورام (الورم) والإيدز. ليس من غير المألوف أن يبدأ الناس في نمو الثآليل. يعلم الجميع كيف أنهم غالبًا ما "يكتسحون" الشفاه وأجنحة الأنف بعد الإصابة بنزلة برد. وهذه كلها أمراض فيروسية. لقد وجد العلماء أن العديد من الفيروسات تعيش في جسم الإنسان، لكنها لا تظهر نفسها دائمًا. فقط الجسم الضعيف هو الذي يكون عرضة لتأثيرات الفيروس الممرض. تختلف طرق الإصابة بالفيروسات اختلافًا كبيرًا: عن طريق الجلد عن طريق لدغات الحشرات والقراد؛ عن طريق اللعاب والمخاط وإفرازات المريض الأخرى؛ عبر الهواء؛ مع الطعام جنسيا وغيرها.
تعد عدوى الرذاذ هي الطريقة الأكثر شيوعًا لنشر أمراض الجهاز التنفسي. يؤدي السعال والعطس إلى إطلاق ملايين القطرات الصغيرة من السوائل (المخاط واللعاب) في الهواء. ويمكن أن يتم استنشاق هذه القطرات، بالإضافة إلى الكائنات الحية الدقيقة التي تحتوي عليها، من قبل أشخاص آخرين. في الحيوانات، تسبب الفيروسات مرض الحمى القلاعية، والطاعون، وداء الكلب؛ في الحشرات - تعدد التعرق، الورم الحبيبي. في النباتات - الفسيفساء أو غيرها من التغييرات في لون الأوراق أو الزهور، حليقة الأوراق وغيرها من التغييرات في الشكل، والتقزم. وأخيرا، في البكتيريا - اضمحلالها. استمرت فكرة اعتبار الفيروسات "مدمرات" لا تتوقف عند أي شيء، في دراسة مجموعة خاصة من الفيروسات التي تصيب البكتيريا. نحن نتحدث عن العاثيات. ويمكن استخدام قدرة العاثيات على تدمير البكتيريا في علاج بعض الأمراض التي تسببها هذه البكتيريا. لقد أصبحت العاثيات بالفعل أول مجموعة من الفيروسات "يروضها" البشر. لقد تعاملوا بسرعة وبلا رحمة مع أقرب جيرانهم في العالم المصغر. الطاعون والتيفوئيد والدوسنتاريا والكوليرا "ذابت" حرفيًا أمام أعيننا بعد مواجهة هذه الفيروسات. بدأ استخدامها للوقاية من العديد من الأمراض المعدية وعلاجها، ولكن لسوء الحظ، أعقب النجاحات الأولى إخفاقات. كان هذا بسبب حقيقة أن العاثيات في جسم الإنسان لم تهاجم البكتيريا بشكل نشط كما هو الحال في أنبوب الاختبار. بالإضافة إلى ذلك، تبين أن البكتيريا "ماكرة" من أعدائها: فقد تكيفت بسرعة كبيرة مع العاثيات وأصبحت غير حساسة لعملها.
بعد اكتشاف المضادات الحيوية، تراجعت العاثيات إلى الخلفية كدواء، لكنها لا تزال تستخدم بنجاح للتعرف على البكتيريا. والحقيقة هي أن العاثيات يمكنها العثور بدقة شديدة على "البكتيريا الخاصة بها" وحلها بسرعة. شكلت الخصائص المماثلة للعاثيات الأساس للتشخيص العلاجي. يتم ذلك عادة على النحو التالي: تنمو البكتيريا المعزولة من جسم المريض على وسط غذائي صلب، وبعد ذلك يتم تطبيق العاثيات المختلفة على "العشب" الناتج، على سبيل المثال الزحار والتيفوئيد. وبعد يوم، يتم فحص الأطباق تحت الضوء وتحديد العاثيات التي تسببت في تحلل البكتيريا. إذا كان لعاثية الزحار مثل هذا التأثير، فسيتم عزل بكتيريا الزحار من جسم المريض، وإذا كان التيفوئيد، فسيتم عزل بكتيريا التيفوئيد.
في بعض الأحيان تأتي الفيروسات التي تصيب الحيوانات والحشرات لمساعدة البشر. منذ أكثر من عشرين عاما في أستراليا، أصبحت مشكلة مكافحة الأرانب البرية حادة. وقد وصل عدد هذه القوارض إلى أبعاد مثيرة للقلق. لقد دمروا المحاصيل بشكل أسرع من الجراد وأصبحوا كارثة وطنية حقيقية. تبين أن الأساليب التقليدية للتعامل معهم غير فعالة. ثم أطلق العلماء فيروسًا خاصًا لمحاربة الأرانب قادر على تدمير جميع الحيوانات المصابة تقريبًا. ولكن كيف ينتشر هذا المرض بين الأرانب الخجولة والحذرة؟ ساعد البعوض. لقد لعبوا دور "الإبر الطائرة"، حيث نشروا الفيروس من أرنب إلى أرنب. وفي الوقت نفسه، ظل البعوض بصحة جيدة تمامًا.
هناك أمثلة أخرى على الاستخدام الناجح للفيروسات لقتل الآفات. يعلم الجميع الأضرار التي تسببها اليرقات والمنشار. الأول يأكل أوراق النباتات المفيدة، والثاني يصيب الأشجار في الحدائق والغابات. ويحاربها ما يسمى بفيروسات التعرق المتعدد والحبيبات، والتي يتم رشها في مناطق صغيرة بالرذاذات، وتستخدم الطائرات لعلاج مساحات واسعة. وقد تم ذلك في الولايات المتحدة الأمريكية عند مكافحة اليرقات التي تصيب حقول البرسيم، وفي كندا عند تدمير ذبابة الصنوبر.
ماذا يحدث للخلية إذا كانت مصابة ليس بفيروس واحد، بل بفيروسين؟ فإذا قررت أنه في هذه الحالة سيتفاقم مرض الخلية ويتسارع موتها، فأنت مخطئ. اتضح أن وجود فيروس واحد في الخلية غالبًا ما يحميها بشكل موثوق من التأثيرات المدمرة لفيروس آخر. هذه الظاهرة أطلق عليها العلماء اسم التدخل الفيروسي. ويرتبط بإنتاج بروتين خاص - الإنترفيرون، والذي ينشط في الخلايا آلية وقائية يمكنها التمييز بين الفيروس وغير الفيروسي وقمع الفيروس بشكل انتقائي. يمنع الإنترفيرون تكاثر معظم الفيروسات في الخلايا. الانترفيرون، الذي يتم إنتاجه كدواء علاجي، يستخدم الآن لعلاج والوقاية من العديد من الأمراض الفيروسية.
V بعض الأمراض الفيروسية البشرية الأكثر شهرة
تظل الأنفلونزا "ملك" الأوبئة. لا يمكن لأي مرض أن يصل إلى مئات الملايين من الناس في وقت قصير، وأكثر من مليار شخص يصابون بالأنفلونزا أثناء الوباء! لم يكن هذا هو الحال خلال جائحة عام 1918 الذي لا يُنسى فحسب، بل كان هذا هو الحال مؤخرًا نسبيًا - في عام 1957، عندما اندلع جائحة الأنفلونزا "الآسيوية"، وفي عام 1968، عندما ظهرت أنفلونزا "هونج كونج". هناك عدة أنواع من فيروسات الأنفلونزا معروفة - A، B، C، إلخ. تحت تأثير العوامل البيئية، قد يزيد عددها. ونظرًا لأن المناعة ضد الأنفلونزا تكون قصيرة المدى ومحددة، فمن الممكن تكرار المرض في موسم واحد. وتشير الإحصائيات إلى أن ما بين 20 إلى 35% من السكان يصابون بالأنفلونزا كل عام.
الجدري هو أحد أقدم الأمراض. تم العثور على وصف للجدري في ورق البردي المصري لأمينوفيس الأول، الذي تم تجميعه عام 4000 قبل الميلاد. تم الحفاظ على آفات الجدري على جلد مومياء مدفونة في مصر 3000 قبل الميلاد. إن ذكر الجدري، الذي أطلق عليه الصينيون "السم من ثدي الأم"، موجود في أقدم مصدر صيني - أطروحة "Cheu-Cheufa" (1120 قبل الميلاد). أول وصف كلاسيكي للجدري قدمه الطبيب العربي الرازي.
الجدول 1-خصائص الأمراض
الإيدز هو مرض معد جديد يعتبره الخبراء أول وباء عالمي حقيقي في تاريخ البشرية المعروف. ولا يشكل الطاعون ولا الجدري ولا الكوليرا سابقة، لأن الإيدز لا يشبه بالتأكيد أيًا من هذه الأمراض وغيرها من الأمراض البشرية المعروفة.
|
اسم المرض |
العوامل الممرضة |
مناطق الجسم المتضررة |
طريقة التوزيع |
نوع التطعيم |
|
الفيروس المخاطي من أحد الأنواع الثلاثة - A وB وC - بدرجات متفاوتة من الفوعة |
الجهاز التنفسي: ظهارة تبطن القصبة الهوائية والشعب الهوائية |
قطرة عدوى |
الفيروس المقتول: يجب أن تتطابق سلالة الفيروس المقتول مع سلالة الفيروس المسبب استمرار الجدول 1 مرض |
|
|
بارد |
مجموعة متنوعة من الفيروسات، غالبًا ما تكون الفيروسات الأنفية (فيروسات تحتوي على RNA) |
مجرى الهواء: عادة العلوي فقط |
قطرة عدوى |
يتم إعطاء الفيروس الحي أو المعطل عن طريق الحقن العضلي. التطعيم ليس فعالًا جدًا نظرًا لوجود العديد من سلالات الفيروسات الأنفية المختلفة |
|
فيروس الجدري (فيروس يحتوي على الحمض النووي)، أحد فيروسات الجدري |
الخطوط الجوية، ثم الجلد |
عدوى القطرات (احتمال انتقال العدوى من خلال جروح الجلد). |
يتم إدخال فيروس حي مضعف (موهن) في خدش الجلد؛ لا تطبق حاليا. |
|
|
النكاف (التهاب النظير) |
الجهاز التنفسي، ثم تعميم العدوى في جميع أنحاء الجسم عن طريق الدم؛ تتأثر بشكل خاص الغدد اللعابية، وعند الرجال البالغين أيضًا الخصيتين |
عدوى الرذاذ (أو انتقال العدوى عن طريق الفم عن طريق اللعاب المُعدي) |
فيروس حي مضعف |
|
|
فيروس الباراميكسوفيروس (فيروس يحتوي على الحمض النووي الريبوزي) |
الجهاز التنفسي (من تجويف الفم إلى القصبات الهوائية)، ثم يمر إلى الجلد والأمعاء |
قطرة عدوى |
فيروس حي مضعف |
|
|
الحصبة الألمانية (الحصبة الألمانية) |
فيروس الحصبة الألمانية |
الخطوط الجوية والغدد الليمفاوية العنقية والعينين والجلد |
قطرة عدوى |
فيروس حي مضعف |
|
شلل الأطفال (شلل الأطفال) |
فيروس شلل الأطفال (فيروس بيكورنا؛ فيروس يحتوي على الحمض النووي الريبوزي، ثلاث سلالات معروفة) |
الحلق والأمعاء ثم الدم. في بعض الأحيان الخلايا العصبية الحركية في النخاع الشوكي، ثم قد يحدث الشلل |
العدوى بالقطرات أو عن طريق البراز البشري |
يُعطى الفيروس الحي الموهن عن طريق الفم، عادة على مكعب سكر |
سادسا: هل الفيروسات حية؟
يتم النظر في وجهتي نظر:
- إذا نظرنا إلى بنية حية تحتوي على أحماض نووية وقادرة على إعادة إنتاج نفسها، فيمكننا قبول وجهة النظر القائلة بأن الفيروسات كائنات حية؛
- إذا افترضنا أن البنية التي لها بنية خلوية هي الوحيدة التي تكون حية، فإن الفيروسات هي شكل غير حي من المادة (البوليمرات).
A. Lehninger في "الكيمياء الحيوية" يعتبر الفيروسات هياكل تقف على عتبة الحياة وتمثل مجمعات فوق جزيئية مستقرة تحتوي على جزيء حمض نووي وعدد كبير من الوحدات الفرعية البروتينية، مرتبة بترتيب معين وتشكل بنية محددة ثلاثية الأبعاد. ومن أهم خصائص الفيروسات يقول:
- عدم القدرة على التكاثر الذاتي في شكل أدوية نقية؛
- القدرة على التحكم في تكرارها (الخلية المصابة)؛
- هناك اختلافات واسعة في الفيروسات من حيث الحجم والشكل والتركيب الكيميائي.
تقع الفيروسات على الحدود بين الكائنات الحية وغير الحية. ويشير ذلك إلى وجود طيف متواصل من العالم العضوي المتزايد التعقيد، والذي يبدأ بجزيئات بسيطة وينتهي بأكثر أنظمة الخلايا تعقيدا.
إن الحجر، وكذلك قطرة السائل التي تحدث فيها عمليات التمثيل الغذائي، ولكنها لا تحتوي على مادة وراثية وغير قادرة على التكاثر الذاتي، هي بلا شك كائن غير حي. البكتيريا كائن حي، وعلى الرغم من أنها تتكون من خلية واحدة فقط، إلا أنها تستطيع إنتاج الطاقة وتصنيع المواد التي تضمن وجودها وتكاثرها. ماذا يمكن أن يقال عن البذرة في هذا السياق؟ ليست كل بذرة تظهر عليها علامات الحياة. ومع ذلك، كونه في حالة سكون، فإنه يحتوي على الإمكانات التي تلقاها من مادة حية بلا شك والتي يمكن تحقيقها في ظل ظروف معينة. وفي الوقت نفسه، يمكن تدمير البذرة بشكل لا رجعة فيه، ومن ثم ستظل الإمكانات غير محققة. وفي هذا الصدد، فإن الفيروس يشبه البذرة أكثر من كونه خلية حية: فهو يتمتع بقدرات معينة قد لا تتحقق، لكنه لا يملك القدرة على الوجود بشكل مستقل.
ولا تعمل الجينات أو البروتينات الخلوية أو الفيروسية في حد ذاتها كمادة حية، والخلية التي لا تحتوي على نواة تشبه الشخص مقطوع الرأس من حيث أنها لا تحتوي على مستوى حرج من التعقيد. كما أن الفيروس غير قادر على الوصول إلى هذا المستوى. لذلك يمكن تعريف الحياة على أنها نوع من الحالة الناشئة المعقدة، بما في ذلك "لبنات البناء" الأساسية نفسها التي يمتلكها الفيروس. إذا اتبعنا هذا المنطق، فإن الفيروسات، التي لا تعتبر كائنات حية بالمعنى الدقيق للكلمة، لا يمكن تصنيفها على أنها أنظمة خاملة: فهي على الحدود بين الكائنات الحية وغير الحية.
سابعا العيش إلى الأبد
الفيروسات التي تحتل موقعًا متوسطًا بين الكائنات الحية وغير الحية تظهر خصائص غير متوقعة. وهنا واحد منهم. عادة، تتكاثر الفيروسات في الخلايا الحية فقط، ولكنها يمكن أن تنمو أيضًا في الخلايا الميتة، وفي بعض الأحيان تعيد الأخيرة إلى الحياة. ومن المثير للدهشة أن بعض الفيروسات، عند تدميرها، يمكن أن تولد من جديد "لحياة مستعارة".
إن الخلية التي تم تدمير حمضها النووي هي خلية "ميتة" حقًا: فهي محرومة من المادة الوراثية مع تعليمات للنشاط. لكن الفيروس يمكنه استخدام مكونات الخلية السليمة المتبقية والسيتوبلازم لتكاثره. إنه يُخضع الجهاز الخلوي ويجبره على استخدام الجينات الفيروسية كمصدر للتعليمات لتخليق البروتينات الفيروسية وتكرار الجينوم الفيروسي. تتجلى القدرة الفريدة للفيروسات على التطور في الخلايا الميتة بشكل واضح عندما يكون المضيف كائنات وحيدة الخلية، خاصة تلك التي تعيش في المحيطات.
الشكل 4. فيروس فسيفساء التبغ
غالبًا ما يتم قتل البكتيريا والبكتيريا الزرقاء التي تقوم بالتمثيل الضوئي والطحالب، وهي المضيفات المحتملة للفيروسات البحرية، بواسطة الأشعة فوق البنفسجية، التي تدمر الحمض النووي الخاص بها. وفي الوقت نفسه، تقوم بعض الفيروسات ("المقيمة" في الكائنات الحية) بتشغيل آلية تخليق الإنزيمات التي تعمل على استعادة الجزيئات التالفة في الخلية المضيفة وإعادتها إلى الحياة. على سبيل المثال، تحتوي البكتيريا الزرقاء على إنزيم يشارك في عملية التمثيل الضوئي، وعندما يتعرض للضوء الزائد، يتم تدميره أحيانًا، مما يؤدي إلى موت الخلايا. وبعد ذلك، تقوم فيروسات تسمى العاثيات الزرقاء "بتشغيل" تخليق نظير لإنزيم التمثيل الضوئي البكتيري، وهو أكثر مقاومة للأشعة فوق البنفسجية. إذا أصاب مثل هذا الفيروس خلية ميتة حديثًا، فيمكن لإنزيم التمثيل الضوئي أن يعيدها إلى الحياة. وهكذا يلعب الفيروس دور "الإنعاش الجيني".
يمكن أن تؤدي الجرعات المفرطة من الأشعة فوق البنفسجية إلى موت العاثيات الزرقاء، لكنها في بعض الأحيان تتمكن من العودة إلى الحياة بمساعدة إصلاحات متعددة. عادة ما تكون هناك عدة فيروسات موجودة في كل خلية مضيفة، وفي حالة تلفها، يمكنها تجميع الجينوم الفيروسي قطعة قطعة. يمكن أن تعمل أجزاء مختلفة من الجينوم كمورد للجينات الفردية، والتي ستعيد، مع جينات أخرى، وظائف الجينوم بالكامل دون إنشاء فيروس كامل. الفيروسات هي الكائنات الحية الوحيدة التي، مثل طائر الفينيق، يمكن أن تولد من جديد من الرماد.
بالتعاون مع زملاء في معهد العلوم الصحية للقاحات والعلاج الجيني بجامعة أوريغون، نقترح أن هناك طريقة ثالثة: كانت الجينات في البداية ذات أصول فيروسية، ولكنها استعمرت بعد ذلك أعضاء من سلالتين مختلفتين من الكائنات الحية، مثل البكتيريا والفقاريات. ومن الممكن أن يكون الجين الذي وهبته البكتيريا للبشرية قد انتقل إلى السلالتين المذكورتين بواسطة الفيروس.
الشكل 5. فيروس اللسان الأزرق
علاوة على ذلك، نحن واثقون من أن نواة الخلية نفسها ذات أصل فيروسي. لا يمكن تفسير ظهور النواة بالتكيف التدريجي للكائنات بدائية النواة مع الظروف المتغيرة. ومن الممكن أن تكون قد تشكلت على أساس الحمض النووي الفيروسي الموجود مسبقًا ذو الوزن الجزيئي العالي، والذي بنى "موطنًا" دائمًا لنفسه داخل الخلية بدائية النواة. وهذا ما تؤكده حقيقة أن جين بوليميريز الحمض النووي للعاثية T4 (العاثيات هي فيروسات تصيب البكتيريا) قريب في تسلسل النوكليوتيدات الخاص به من جينات بوليميريز الحمض النووي لكل من حقيقيات النوى والفيروسات التي تصيبها. بالإضافة إلى ذلك، توصل باتريك فورتير من جامعة باريس الجنوبية، الذي درس الإنزيمات المشاركة في تكرار الحمض النووي، إلى استنتاج مفاده أن الجينات التي تحدد تركيبها في حقيقيات النوى هي من أصل فيروسي.
تؤثر الفيروسات على جميع أشكال الحياة على الأرض، وغالبًا ما تحدد مصيرها. وفي الوقت نفسه، فإنها تتطور أيضًا. ويأتي الدليل المباشر من ظهور فيروسات جديدة، مثل فيروس نقص المناعة البشرية (HIV)، الذي يسبب مرض الإيدز.
تقوم الفيروسات باستمرار بتعديل الحدود بين العالمين البيولوجي والكيميائي الحيوي. كلما تقدمنا في دراسة جينومات الكائنات الحية المختلفة، كلما وجدنا أدلة أكثر على وجود جينات من مجموعة ديناميكية قديمة جدًا. تحدث سلفادور لوريا الحائز على جائزة نوبل عن تأثير الفيروسات على التطور عام 1969: "ربما كانت الفيروسات، بقدرتها على الدخول والخروج من الجينوم الخلوي، مشاركين نشطين في عملية تحسين المادة الوراثية لجميع الكائنات الحية أثناء التطور. ببساطة لم نلاحظ ذلك". بغض النظر عن العالم - الحي أو غير الحي - الذي ننسب إليه الفيروسات، فقد حان الوقت للنظر فيها ليس بمعزل عن غيرها، ولكن مع مراعاة ارتباطها المستمر بالكائنات الحية.
خاتمة
ترتبط مكافحة الالتهابات الفيروسية بالعديد من الصعوبات، من بينها مناعة الفيروسات للمضادات الحيوية. تتحور الفيروسات بشكل نشط، وتظهر بانتظام سلالات جديدة لم يتم العثور على "أسلحة" ضدها بعد. بادئ ذي بدء، ينطبق هذا على فيروسات الحمض النووي الريبوزي (RNA)، التي عادة ما يكون جينومها أكبر، وبالتالي أقل استقرارًا. حتى الآن، تتطور مكافحة العديد من الالتهابات الفيروسية لصالح البشر، ويرجع ذلك أساسًا إلى التطعيم الشامل للسكان لأغراض وقائية. أدت مثل هذه الأحداث في النهاية إلى حقيقة أن فيروس الجدري، وفقًا للخبراء، قد اختفى الآن من الطبيعة. نتيجة للتطعيم الشامل في بلادنا عام 1961. وتم القضاء على وباء شلل الأطفال. إلا أن الطبيعة لا تزال تختبر الإنسان، من وقت لآخر، وتقدم المفاجآت على شكل فيروسات جديدة تسبب أمراضاً فظيعة. والمثال الأكثر وضوحا هو فيروس نقص المناعة البشرية، الذي لا يزال البشر يخسرون المعركة ضده. انتشاره يتوافق بالفعل مع الوباء.
مهم! تهدف جميع الملخصات المقدمة للتنزيل المجاني إلى وضع خطة أو أساس لأعمالك العلمية.
أصدقاء! لديك فرصة فريدة لمساعدة الطلاب مثلك تمامًا! إذا ساعدك موقعنا في العثور على الوظيفة التي تحتاجها، فمن المؤكد أنك تفهم كيف يمكن للوظيفة التي تضيفها أن تجعل عمل الآخرين أسهل.
إذا كان الملخص، في رأيك، ذو جودة رديئة، أو كنت قد شاهدت هذا العمل بالفعل، فيرجى إخبارنا بذلك.
ويعتقد أن الفيروسات (من اللات. فايروس- السم) - شيء قبيح لا يجلب إلا المتاعب. لكن هذا خطأ فادح. الفيروسات هي المبدعين الرئيسيين للطبيعة الحية ومحركات تطورها.
إحدى الحجج الرئيسية ضد الفرضية القائلة بأن الفيروسات "هربت" من الخلايا هي حقيقة أن الأنظمة الوراثية الفيروسية أكثر تنوعًا من الأنظمة الخلوية. كما هو معروف، فإن الكائنات الخلوية تحتوي فقط على جينومات DNA مزدوجة الجديلة - خطية أو دائرية. ويمكن تمثيل جينوم الفيروس بجزيئات الحمض النووي الريبوزي (RNA) أو الحمض النووي (DNA) المفردة والمزدوجة، سواء كانت خطية أو دائرية. هناك أيضًا أنظمة تستخدم النسخ العكسي. وهكذا، في الفيروسات القهقرية (على سبيل المثال، بعض الفيروسات الورمية، فيروس نقص المناعة البشرية) والفيروسات نظيرة القهقرية (فيروسات التهاب الكبد B، فسيفساء القرنبيط، وما إلى ذلك)، يتم تصنيع إحدى سلاسل الحمض النووي الجيني في قالب الحمض النووي الريبي (RNA). الفيروسات، على عكس الكائنات الخلوية، تنفذ جميع الطرق الممكنة نظريًا لتخزين المعلومات الجينية والتعبير عنها.
الحجة المهمة الثانية ضد اعتبار الفيروسات ناشئة عن الخلايا هي أن هناك العديد من الجينات الفيروسية غير الموجودة في الكائنات الخلوية. لم تتطور الكائنات الخلوية من الفيروسات فحسب، بل ورثت أيضًا (وما زالت ترث) جزءًا كبيرًا من مادتها الجينية منها. ومما يثير الاهتمام بشكل خاص في هذا الصدد الفيروسات الداخلية (أجزاء من جينوم الحمض النووي الريبوزي (RNA) أو فيروسات الحمض النووي المدمجة في جينوم الخلية)، ومن بينها تسود الجينات المشتقة من الفيروسات القهقرية. يُعتقد أن الثدييات ورثت أكثر من نصف الجينوم الخاص بها من الفيروسات وأقرب أقربائها - العناصر الوراثية "الأنانية"، مثل البلازميدات والترانسبوزونات. وبالتالي، فإن الفيروسات هي آباء البشر. في كثير من الأحيان يتم تغيير التسلسل الجيني للفيروسات الداخلية، والتي توجد بأعداد كبيرة في الجينوم البشري، ولا تعد ترمز للبروتينات. هناك سبب وجيه للاعتقاد بأن مثل هذه التسلسلات تشارك في تنظيم الجينات الخلوية، على الرغم من أن وظائفها البيولوجية المحددة غالبًا ما تكون غير معروفة. ومع ذلك، فإننا نعرف شيئًا مهمًا: على سبيل المثال، بروتين سينسيتين، الذي يتم تشفيره بواسطة الجين المغلف لأحد الفيروسات القهقرية الذاتية، ضروري لدمج الخلايا أثناء تكوين المشيمة. وهذا يعني أنه لا يمكن أن يولد البشر ولا الحيوانات المشيمية بدون هذا الفيروس الداخلي. هناك مثال مهم آخر. اتضح أن أحد مكونات جينوم أحد الفيروسات الداخلية يتحكم في التعبير عن هيدروجيناز البرولين في بعض مناطق الجهاز العصبي المركزي. ربما لعب هذا الإنزيم دورًا مهمًا في تطور الدماغ البشري. وإذا تعطل التعبير عن هذا الإنزيم نتيجة الطفرات، تحدث أمراض نفسية، بما في ذلك الفصام. تلعب الفيروسات وأقاربها أيضًا دورًا مهمًا في النقل الأفقي للجينات الخلوية - من كائن حي إلى آخر.
ومع ذلك، على الرغم من دورها الرئيسي في التطور، تُعرف الفيروسات بأنها مسببات الأمراض للإنسان والحيوان والنبات (بالمناسبة، هذا هو سبب اكتشافها لأول مرة). وبعد ذلك سنتحدث عن طبيعة المرضية الفيروسية. الفيروسات (وخاصة الفيروسات حقيقية النواة) ليس لديها "رغبة" خاصة في إيذاء المضيف، ناهيك عن قتله. وفي كثير من الحالات، تتعايش الفيروسات بشكل سلمي وودود مع الخلايا. لماذا الكثير من الفيروسات ضارة جدًا؟ التفسير المعتاد هو أن أمراض الخلية المصابة ناتجة عن "نهب" مواردها (المادية والهيكلية)، والتي يوجهها الفيروس إلى احتياجاته الخاصة للتكاثر. ومع ذلك، يمكن أن يحدث الضرر الأكبر من الإجراءات الوقائية غير الحكيمة التي يقوم بها المضيفون والنشاط الوقائي للفيروسات، والذي لا يرتبط مباشرة بتكاثرها.
آليات الحماية والدفاع المضاد
ما هي آليات الدفاع الرئيسية للخلية المصابة؟ هذه هي مكونات المناعة الفطرية: تدهور الحمض النووي الريبي (الفيروسي والخلوي)، وتثبيط تخليق البروتين (سواء الفيروسي أو الخلوي)، والتدمير الذاتي (موت الخلايا المبرمج وأنواع أخرى من الموت المبرمج)، وأخيرا، الالتهاب. في الواقع، العديد من الفيروسات اكتشفت وجودها بهذه الطريقة - بسبب الالتهابات التي تسببها (التهاب الدماغ والالتهاب الرئوي وغيرها). تحارب الخلية الفيروس عن طريق تعطيل عملية التمثيل الغذائي و/أو البنية الخاصة بها، وعادةً ما تكون آليات الدفاع الخاصة بها ضارة ذاتيًا. يمكنك القول أن الشخص الذي يموت بسبب مرض شلل الأطفال (وأقل من 1٪ يموتون) قتل نفسه أثناء مكافحة العدوى.
استجابة للدفاعات الخلوية، تتطور الفيروسات لتطوير الدفاعات، ويحدث سباق تسلح بين الفيروس والخلية. يتم توجيه هذه الأدوية بشكل أساسي ضد العمليات الأيضية العامة التي تقوم عليها التفاعلات الدفاعية للخلية. وهذا مرة أخرى هو تثبيط تخليق الحمض النووي الريبي (RNA) الخلوي والبروتينات، وتعطيل البنية التحتية داخل الخلايا ونقل الخلايا، أو قمعها، أو على العكس من ذلك، إطلاق موت الخلايا المبرمج والآليات الأخرى التي تسبب موت الخلايا المبرمج. وبالتالي، فإن استراتيجية الدفاع عن الفيروس تشبه في كثير من النواحي السلوك الدفاعي للخلية. من الناحية المجازية، يستخدم المصارعون نفس الأساليب ويحققون نفس الأهداف. على سبيل المثال، تستخدم الخلية، التي تثبط تخليق البروتينات الفيروسية، الإنترفيرون، ولمنع تكوينه، يقوم الفيروس بدوره بتثبيط تخليق البروتين في الخلية. اعتمادًا على الظروف، يستفيد جانب أو آخر. اتضح أن المساهمة الرئيسية في علم الأمراض ليست تكاثر الفيروس في حد ذاته، ولكن المواجهة بين الدفاع الخلوي والدفاع الفيروسي. في علم أمراض النبات، كان مفهوم "التسامح" موجودًا منذ فترة طويلة: يمكن للفيروس الممرض أن يتكاثر بشكل نشط في النبات المصاب دون التسبب في أعراض مؤلمة.
أدناه سنتحدث بشكل أساسي عن فيروسات الحمض النووي الريبوزي (وهذا مثال أبسط). كيف يكشف فيروس RNA، بمجرد دخوله إلى الخلية، عن وجوده؟ وكيف تعرف الخلية أن الفيروس دخل إليها؟ السمة الرئيسية التي "تفهمها" الخلية هي الحمض النووي الريبي الفيروسي المزدوج الذي تقطعت به السبل، والذي، من حيث المبدأ، يمكن تشكيله في خلية غير مصابة، ولكن ليس بهذه الكميات والأماكن. في بعض الحالات، تتعرف الخلية أيضًا على الحمض النووي الريبي الفيروسي المفرد الذي تقطعت به السبل، وأحيانًا (في كثير من الأحيان) البروتينات الفيروسية. من المهم أن يكون التعرف على الحمض النووي الريبوزي الفيروسي غير محدد: فبعد أن "استشعرت" الحمض النووي الريبي المزدوج الشريط، قد "تعتقد" الخلية أن فيروسًا قد دخل إليها، لكنها لا تعرف أي فيروس. يتم التقاط الحمض النووي الريبي (RNA) بواسطة نوعين من أجهزة الاستشعار: Toll-like (من الإنجليزية. مثل الرسومومنه. رسوم- رائعة) المستقبلات ومروحيات الحمض النووي الريبي المتخصصة. أنها تنطوي على عدد من آليات الحماية على المستوى النسخي، بما في ذلك تشكيل الإنترفيرون. بالإضافة إلى ذلك، يتم التعرف على الحمض النووي الريبوزي الفيروسي من قبل "المنفذين" - بروتين كيناز PKR المعتمد على الحمض النووي الريبي المزدوج، والذي يفسفر بعض عوامل بدء الترجمة، وبالتالي يثبط تخليق البروتين؛ إنزيم أوليجوادينيلات (OAS)، الذي ينشط RNase L، الذي يقسم الحمض النووي الريبي (RNA)؛ نظام تداخل الحمض النووي الريبوزي (RNA)، مما يؤدي إلى تدهور الحمض النووي الريبي (RNA) وتعطيل ترجمته.
ولأن الفيروس يتم التعرف عليه كشيء غير محدد، فإن الخلية لا تستطيع معرفة "نواياها". وبشكل عام، سيكون من المستحيل التوصل إلى نظام دفاع فطري فردي ضد أي فيروس محتمل. وهذا يعني أن الخلية لا يمكنها محاربة الفيروس إلا بالتقنيات القياسية. وبالتالي، فإن تصرفاتها الدفاعية غالباً ما تكون غير متناسبة مع التهديد القائم. ومع ذلك، إذا كانت ردود الفعل الدفاعية للخلية غير محددة إلى هذا الحد، فلماذا لا تزال الفيروسات المختلفة تسبب أمراضًا مختلفة؟ أولا، يمكن لكل فيروس أن يصيب فقط نوع معين من الخلايا في كائن حي معين. ويرجع ذلك إلى حقيقة أنه لكي تتمكن من اختراق الخلية، يجب أن تتفاعل مع المستقبلات الخلوية "المناسبة" لها. بالإضافة إلى ذلك، لتكاثر الفيروسات، هناك حاجة إلى بيئة معينة داخل الخلايا (غالبًا ما تكون هناك حاجة إلى بروتينات خلوية محددة). ثانيا، في حين أن ردود الفعل الدفاعية للخلية قياسية، فإن دفاعات الفيروس تكون فردية إلى حد كبير، على الرغم من أنها موجهة ضد الآليات الخلوية القياسية.
في النباتات، يلعب تدخل الحمض النووي الريبي (RNA) دورًا مهمًا جدًا كآلية مضادة للفيروسات. يتكون الحمض النووي الريبي المزدوج تقطعت بهم السبل من الحمض النووي الريبي الفيروسي (عامل مهم تتعلم من خلاله الخلية عن وجود الفيروس). بمشاركة مكونات نظام تداخل الحمض النووي الريبي (RNA) - إنزيم Dicer، الذي يقطع هذا الحمض النووي الريبي المزدوج الذي تقطعت به السبل إلى أجزاء من 21-25 زوجًا من النوكليوتيدات في الطول، ثم مجمع بروتين الحمض النووي الريبي (RISC) - يتم في النهاية شظايا الحمض النووي الريبي (RNA) القصيرة المفردة التي تقطعت بهم السبل شكلت. من خلال تهجينها مع الحمض النووي الريبوزي الفيروسي (RNA) الفيروسي، فإنها تسبب إما تدهوره أو تثبيط ترجمته. تعتبر آلية الحماية هذه فعالة، ولكنها يمكن أن تلحق الضرر بالخلية نفسها، كما يظهر بوضوح في مثال أشباه الفيروسات. هذه هي مسببات الأمراض النباتية، وهي عبارة عن جزيئات RNA دائرية قصيرة (عدة مئات من النيوكليوتيدات) غير مغطاة بقشرة بروتينية. لا ترمز أشباه الفيروسات إلى البروتينات ولكنها يمكن أن تسبب أعراضًا حادة في النبات المصاب. يحدث هذا لأن الخلية تحمي نفسها. يتم تعريض الحمض النووي الريبي المزدوج الفيروسي الناتج لجميع مكونات نظام تداخل الحمض النووي الريبي (RNA)، مما يؤدي إلى تكوين شظايا الحمض النووي الريبي (RNA) المفردة الذين تقطعت بهم السبل والتي لا تهجن مع الحمض النووي الريبي الفيروسي، ولكن مع الحمض النووي الريبي الخلوي. وهذا يؤدي إلى تدهورها وتطور أعراض المرض. ومع ذلك، فإن العديد من الفيروسات النباتية تقوم بتشفير مجموعة متنوعة من البروتينات التي تتداخل مع تداخل الحمض النووي الريبي (RNA) ( المثبطات الفيروسية لإسكات الحمض النووي الريبي (RNA) - VSR). فهي إما تمنع التعرف على RNA الفيروسي وانقسامه، أو تمنع تكوين وعمل مجمع RISC. لذلك، يمكن لبروتينات VSR هذه أن تعطل آليات تدخل الحمض النووي الريبي (RNA) المهمة من الناحية الفسيولوجية (غير الفيروسية)، مما يسبب أعراض مرضية.
البروتينات الأمنية
يعتمد الدفاع عن الفيروسات، وخاصة الفيروسات البيكورناوية، ومسببات الأمراض الصغيرة التي تحتوي على الحمض النووي الريبي (RNA)، إلى حد كبير على عمل هذه البروتينات. وتشمل هذه المجموعة الكبيرة، على وجه الخصوص، مسببات أمراض شلل الأطفال، والتهاب الكبد الوبائي أ، ومرض الحمى القلاعية، وما إلى ذلك. وتكمن خصوصية هذه الفيروسات في أنه، مع استثناءات نادرة، يتم تصنيع بروتيناتها على شكل بروتين متعدد واحد، من والتي يتم بعد ذلك تشكيل البروتينات الفردية الناضجة. من بينها يمكن تمييز ثلاث مجموعات. الأول يتكون من بروتينات رئيسية - حيوية، ذات وظائف ثابتة، تضمن بشكل مباشر تكاثر الفيروس: بوليميرات الحمض النووي الريبي المعتمدة على الحمض النووي الريبي (RNA)، الضرورية لتكرار الجينوم الفيروسي؛ البروتينات القفيصة التي تشكل الغلاف البروتيني للفيروس؛ البروتياز المشاركة في عملية تحويل البروتينات المتعددة إلى بروتينات ناضجة؛ بروتين في بي جي ( ربط جينوم البروتين الفيروسي- بروتين فيروسي متصل بالجينوم) يعمل بمثابة تمهيد لتركيب جزيئات الحمض النووي الريبي (RNA)؛ يعد Helicase إنزيمًا قيمًا للغاية تمتلكه جميع الفيروسات البيكورناوية، لكنه يلعب دورًا غير واضح تمامًا. تشمل المجموعة الثانية أيضًا البروتينات الحيوية، ولكن تلك التي تؤدي عملًا "مساعدًا" - البروتينات "المرشدة" الكارهة للماء 2B و3A. إنهم يوجهون البروتينات الرئيسية إلى وجهاتهم ويساعدون في خلق بيئة مثالية داخل الخلايا لتكاثر الفيروس. أما المجموعة الثالثة فتضم البروتين الرائد L الذي تم اكتشافه في مختبرنا قبل 30 عاماً، والبروتين 2A؛ أطلقنا عليها اسم البروتينات "الأمنية" ( حماية- حماية). هذا هو "سلاح" متخصص مضاد للدفاع من فيروسات بيكورنافيروس. بشكل عام، يمكن لجميع هذه الفئات الثلاثة من البروتينات محاربة آليات الدفاع في الخلية. لكن البروتينات الرئيسية والبروتينات التوجيهية تقوم بهذه المهمة بدوام جزئي لأن لديها مسؤوليات مهمة أخرى يجب أن يستوعبها هيكلها ووظيفتها. وبالتالي، فإن قدراتهم الدفاعية محدودة بسبب الحاجة إلى أداء العمل الأساسي. لكن السناجب "الأمنية" تعمل بدوام كامل في تخصصها - فالتطور "استأجرها" خصيصًا من أجل "الأمن" (لاحقًا "تعلم" بعضها القيام بشيء آخر). يمكن أن يكون لديهم أي هيكل ضروري للقيام بواجباتهم.
ومن أهم وظائف البروتينات الأمنية أنها تشارك في تحديد مصير الخلية المصابة. هناك العديد من الخيارات المختلفة لموتها، ولكن الآليتين الرئيسيتين الأكثر شهرة هما النخر وموت الخلايا المبرمج، واللتان تختلفان في الخصائص المورفولوجية والكيميائية الحيوية. أثناء النخر، يتم تحلل الخلية، ويتم سكب محتوياتها في الفضاء بين الخلايا. أثناء موت الخلايا المبرمج، تتشكل نتوءات مرئية بوضوح على سطحها، ويتحلل الحمض النووي الخاص بها إلى شظايا نووية، وفي النهاية يتم تجزئة الخلية إلى أجسام موت الخلايا المبرمج الفردية تقتصر على غشاء البلازما. من المهم جدًا كيف تموت الخلية بالضبط. مع النخر، يتطور الالتهاب الوقائي، لكن الفيروس يترك الخلية وينتشر. في حالة موت الخلايا المبرمج، يكون انتشار الفيروس محدودًا ولا يوجد عادةً أي تفاعل التهابي. إن موت الخلية المصابة، كقاعدة عامة، هو عمل من أعمال التضحية بالنفس يحد من تكاثر الفيروس.
لقد وجدنا أن العدوى بالفيروسات البيكورناوية، وخاصة فيروس شلل الأطفال (فيروس شلل الأطفال)، تؤدي إلى برنامج موت الخلايا المبرمج. يحدث هذا على طول أحد المسارات الكلاسيكية، عندما يتم إطلاق السيتوكروم من الميتوكوندريا جويتم تنشيط سلسلة من الإنزيمات المحللة للبروتين، الكاسبيز. ولكن، من ناحية أخرى، اتضح أن الفيروسات لديها آلية مضادة لموت الخلايا المبرمج - القدرة على قمع رد فعل موت الخلايا المبرمج للخلية. وهكذا، فإن خلايا هيلا المصابة بفيروس شلل الأطفال أو فيروس التهاب الدماغ والعضلة القلبية (أيضًا فيروس بيكورنا) تموت مع ظهور علامات النخر. ولكن إذا قمت بإيقاف تشغيل "السلاح" المضاد لموت الخلايا المبرمج (قمع تخليق البروتينات الفيروسية)، فإن الخلية تموت من موت الخلايا المبرمج (التضحية بالنفس). وفي كلا الفيروسين، تعمل البروتينات "الأمنية" كأسلحة من هذا القبيل. ومع ذلك، في فيروس التهاب الدماغ والعضلة القلب يلعب هذا الدور البروتين L، وفي فيروس شلل الأطفال هو البروتين 2A. البروتين القائد ليس له نشاط إنزيمي، في حين أن البروتين 2A عبارة عن بروتياز. ليس لديهم أي شيء مشترك سواء من الناحية الهيكلية أو الكيميائية الحيوية، ولكن كلاهما لهما تأثيرات مضادة للخلايا على أساس آليات جزيئية مختلفة.

هناك آلية أخرى مضادة للحماية للبروتينات الأمنية لفيروس بيكورنا وهي تعطيل النقل السيتوبلازمي النووي [10-12]. لقد أظهرنا أنه عند الإصابة بهذه الفيروسات، تزداد نفاذية الغشاء النووي ويتعطل التبادل النشط للجزيئات الكبيرة بين السيتوبلازم والنواة. وإذا تضررت بنية الخلية، فلا يمكنها تشغيل آلياتها التنظيمية لمحاربة الفيروس. في فيروس شلل الأطفال، يعطل البروتين الأمني 2A النقل السيتوبلازمي النووي عن طريق تحليل النيوكليوبورينات، وهي مكونات المسام النووية. ويعمل البروتين الرئيسي لفيروس التهاب الدماغ والعضلة القلب - فهو يؤثر على سلسلة الفسفرة الخلوية للنيوكليوبرينات [،].
يمكن للوظيفة المضادة للحماية للبروتينات "الأمنية" أن تتجلى بطرق أخرى. وهكذا، فإن بروتينات L من فيروسات القلب (بما في ذلك فيروس التهاب الدماغ والعضلة القلب) وبروتينات 2A من الفيروسات المعوية (بما في ذلك فيروس شلل الأطفال) تمنع تكوين الإنترفيرون. ويتم تثبيط تأثيره بواسطة بروتين L لفيروس مرض الحمى القلاعية وبروتين 2A لفيروس شلل الأطفال. ومع ذلك، فإن البروتينات "الأمنية" للفيروسات البيكورناوية ليست حيوية. يمكن إزالة كلا الحارسين أو يمكن أن تحدث عمليات حذف كبيرة فيهما (كما في حالة البروتين L لفيروسات القلب، وبروتينات 2A لفيروس التهاب الكبد A وفيروسات القلب) دون أن يصبح الفيروس قابلاً للحياة.
نزع السلاح المتبادل

ما هي عواقب تعطيل البروتينات "الأمنية" الفيروسية للخلية؟ فمن ناحية، ستزداد حساسية الفيروسات لآليات الحماية للمناعة الخلوية الفطرية. ولكن من ناحية أخرى، فإن نشاطه الانتحاري الذي يؤذي نفسه سيزداد أيضًا. ماذا يحدث إذا قمت في نفس الوقت بإيقاف آليات الدفاع عن الخلية والفيروس؟ قمنا بدراسة هذا الوضع باستخدام مثال التفاعل بين الفيروس السحائي (سلالة من فيروس التهاب الدماغ والعضلة القلب) وخلايا هيلا. بعد إصابتهم بفيروس من النوع البري، يموتون بسرعة من النخر. وإذا تم نزع سلاح الفيروس جزئيا (يتم تعطيل البروتين القائد)، فإن خلايا هيلا تعيش لفترة أطول قليلا ولا تموت من النخر، ولكن من موت الخلايا المبرمج. عندما ينخفض الدفاع المتبادل (يتم إيقاف موت الخلايا المبرمج في الخلية بواسطة مركب كيميائي يثبط الكاسبيز، ويتم تعطيل البروتين الرئيسي للفيروس)، حتى بعد فترة زمنية أطول بمرتين، تشعر الخلايا بتحسن كبير من تلك التي لم تكن كذلك منزوع السلاح. واستمر تكاثر الفيروس (الديناميكية والحصاد) بنفس الطريقة تمامًا، بغض النظر عما إذا كانت دفاعاته فقط قد تم إيقافها أو ما إذا كانت الدفاعات الخلوية قد تمت إزالتها أيضًا في نفس الوقت. اتضح أنه في الخلايا التي لم تتعرض بعد لأضرار مرضية خطيرة (ما يسمى بتأثير الاعتلال الخلوي)، يمكن أن تتشكل بالفعل الكثير من الجزيئات الفيروسية. وبالتالي، فإن تلف الخلايا ليس ضروريًا لتكاثر الفيروس. ولذلك، فإن الإستراتيجية الفعالة للعلاج المضاد للفيروسات التي تهدف إلى تخفيف أعراض المرض قد تكون القمع المتزامن لكل من الدفاعات الفيروسية والخلوية.
الموت المبرمج
أتاحت هذه السلسلة من تجاربنا أيضًا فرصة للتعمق أكثر في طبيعة الموت النخري الناجم عن الفيروس. ما هو قتل الخلية بفيروس أو انتحارها (التضحية بالنفس) عندما تقرر أنه من الأفضل أن تموت من أجل الصالح العام؟ ما يلي عرضة للآفات النخرية:
- غشاء البلازما (تزداد نفاذيته، وتشكل "بثور")،
- السيتوبلازم (تغير الأنابيب الدقيقة والألياف الدقيقة) ،
- النواة (تتقلص، تشوه، يتكثف الكروماتين)،
- النشاط الأيضي (تفاعلات الاختزال المعتمدة على NADH، تغير القدرة على البقاء).
عندما يتم إيقاف موت الخلايا المبرمج (إضافة مثبط كاسباس كيميائي)، تعتمد التغيرات النخرية المختلفة على ما إذا كان البروتين القائد الفيروسي يعمل أم لا. على سبيل المثال، إذا تم تعطيله، فإن نفاذية غشاء الخلية لا تتغير، ولا تظهر "البثور" المرتبطة بخلل في التوازن الأسموزي، ولا يحدث عدد من الآفات النخرية الأخرى. أحد التفسيرات المحتملة لهذا التأثير هو أن بروتين L يعمل على أهداف متعددة في حجرات خلوية مختلفة. ولكن نظرًا لأن البروتين صغير وليس له نشاط إنزيمي، فمن المرجح أن تكون أهدافه المباشرة أصغر بكثير. نحن نفترض أن البروتين القائد يعمل على واحد أو أكثر من العناصر الخلوية الرئيسية التي تتحكم في مصير الخلية، ونتيجة لذلك، يتم إطلاق برنامجها النخري، وهو المسؤول عن معظم التغيرات المرضية المذكورة. وبالتالي، ليس الفيروس هو الذي يقتل الخلية بشكل نخري، بل الخلية نفسها تنتحر (تقوم بعمل من أعمال التضحية بالنفس). تتوافق وجهة النظر هذه مع الأفكار الجديدة، والتي بموجبها، بالإضافة إلى موت الخلايا المبرمج، هناك عدد من الأنواع الأخرى المهمة من الناحية الفسيولوجية لموت الخلايا المبرمج (المشفر في الجينوم الخلوي)، بما في ذلك التنخر، الذي يشبه النخر.
وبالتالي، فإن التضحية الذاتية للخلية أثناء العدوى الفيروسية يمكن أن تظهر على شكل نخر أو موت الخلايا المبرمج. قد يكون تنخر الخلايا بمثابة رد فعل وقائي للخلية تجاه عدوى فيروسية، وليس فقط في حالة فيروسات بيكورنا. تعتمد الآلية الأكثر فائدة للفيروس على الظروف. نرى أن تأثيره المضاد للحماية يمكن أن يتجلى في شكل "إعادة توجيه" للآليات المشفرة في جينوم الخلية. هذه طريقة دفاعية مهمة (وإن لم تكن الوحيدة) وإحدى الآليات الرئيسية لإمراض الفيروسات. تتنافس برامج موت الخلايا المبرمج والنخر الناجم عن الفيروسات مع بعضها البعض. لقد أظهرنا أنه عندما تصاب خلايا هيلا بفيروس شلل الأطفال، يتم تنشيط موت الخلايا المبرمج أولاً، ثم يتم قمعه وإطلاق المسار النخري. وبالتالي، فإن إصابة الخلية بفيروس ينشط فيها عددًا من الإجراءات الوقائية، من بينها آليتان انتحاريتان للموت المبرمج - موت الخلايا المبرمج والنخرية. ومن ثم يحدث التنافس بين هذه المسارات: فقمع أحدهما ينشط الآخر، والعكس صحيح. وكل هذا يتم تنظيمه بواسطة البروتينات الخلوية، والبروتينات الفيروسية (البروتينات "الأمنية" في المقام الأول)، بالإضافة إلى العوامل الخارجية.
سباق التسلح
وبما أن الخلايا لديها آليات دفاعية، والفيروسات لديها آليات دفاعية، فمن الطبيعي أن يكون هناك سباق تسلح بينهما. تشير الطبيعة غير المحافظة للبروتينات الأمنية إلى أنها تم تكييفها لمواجهة آليات الدفاع لمضيف معين. وبالتالي، قد يكون تغيره مصحوبًا بفقدان وظيفة البروتين "الأمنية"، ونتيجة لذلك، زيادة في ردود الفعل الدفاعية للمضيف. وهذا يمكن أن يفسر القدرة المرضية الخاصة لـ "الجديد" ( الناشئة حديثا- الناشئة) الفيروسات. وبالتالي، فإن فيروس الأنفلونزا هو فيروس معوي منخفض الإمراض وغير ضار تقريبًا للطيور البرية. عندما تصيب شخصًا، يمكن أن تحدث الأنفلونزا الإسبانية أو أنفلونزا الطيور أو أنفلونزا الخنازير. ويعتبر فيروس السارس آمنا نسبيا بالنسبة للخفافيش، لكنه يسبب عند البشر متلازمة الجهاز التنفسي الحادة الوخيمة، المصحوبة بارتفاع معدل الوفيات. أخيرا، فيروس نقص المناعة البشرية (على وجه التحديد، سلفه) غير ضار عمليا للقردة، ولكن في البشر يسبب الإيدز. من المهم جدًا ألا تطور هذه الفيروسات عوامل إمراضية جديدة عند الانتقال إلى مضيف جديد (ببساطة، نتيجة للعديد من الطفرات التي تضمن اختراق الخلية، فإنها تكتسب القدرة على إصابة البشر). هناك آلية أخرى محتملة لاختلال التوازن بين الفيروس والمضيف وظهور مسببات أمراض جديدة، وهي حدوث تغيير في أسلحة الدفاع الفيروسية، على سبيل المثال، فقدان سلاح قديم أو الحصول على بروتين "أمني" جديد.
ومع ذلك، فإن التطور المشترك على المدى الطويل للمضيف والفيروس ينبغي أن يؤدي إلى انخفاض في القدرة المرضية لهذا الأخير (نزع السلاح المفيد للطرفين). المثال الكلاسيكي هو فيروس الورم العضلي/الورم الليفي. في منتصف القرن التاسع عشر. تم جلب الأرانب الأوروبية إلى أستراليا، وسرعان ما تضاعفت وأصبحت تشكل تهديدا خطيرا للزراعة. وبعد 100 عام، بدأ استخدام فيروس الورم الليفي/الورم المخاطي الممرض (من عائلة فيروسات الجدري، والتي تشمل فيروس الجدري) للسيطرة على سكانها. تتفاعل الأرانب المختلفة بشكل مختلف مع هذا الفيروس. في الأرانب البرازيلية، بعد ثلاثة أسابيع من الإصابة، يسبب ورمًا حميدًا - ورمًا ليفيًا (عقيدة موضعية على الجلد). لكن الأرانب الأوروبية الحساسة لهذا الفيروس تصاب بمرض قاتل معمم خلال 10 أيام بعد الإصابة.
تسبب الفيروس، الذي تم إدخاله إلى أستراليا، في حدوث أوبئة صيفية ينقلها البعوض، حيث مات أكثر من 99٪ من الأرانب المصابة في أقل من أسبوعين. كانت السلالات الأقل ضراوة من الفيروس أكثر عرضة للبقاء على قيد الحياة في فصل الشتاء، مما أدى إلى اختيار سلالات ضعيفة (موهنة). وبعد حوالي 10 سنوات، انخفض معدل وفيات الأرانب الأوروبية بسبب الفيروس المتطور إلى النصف. وفي الوقت نفسه، تم اختيار الأرانب المقاومة: انخفض معدل الوفيات بسبب الفيروس الأصلي بنحو أربع مرات. وفي عقد واحد فقط (فترة لا تذكر من الناحية التطورية)، تحسنت العلاقة بين العامل الممرض والمضيف بنحو 10 أضعاف. هذا، بالطبع، مخطط مبسط إلى حد ما، لأن سباق التسلح لا يتوقف: استجابة لزيادة المقاومة لدى الأرانب، قد تزداد ضراوة الفيروس أيضًا. إلا أن هذا مثال صارخ على دور تفاعل الفيروسات والكائنات الخلوية في تطور كليهما. "تعلم" الفيروسات والخلايا بعضها البعض، ويتم توريث "المعرفة" المكتسبة. في عام 2013، نشر اثنان من خريجي قسم علم الفيروسات بجامعة موسكو الحكومية، وهما إيفجيني كونين وفاليريان دوليا، مقالًا حول وجهة النظر "المتمركزة حول الفيروس" للتطور، والتي بموجبها تعتبر مقاومة وتعاون الفيروسات والكائنات الخلوية هو العامل الرئيسي في التطور. تطورهم.
قصتي لا تستنفد الموضوع: يُعرف الكثير عن طبيعة القدرة المرضية للفيروسات. إن الكثير مما نعرفه الآن قد تعلمناه في السنوات الأخيرة، وهناك كل الأسباب التي تجعلنا نتوقع مفاجآت جديدة. يمكننا ويجب علينا إلقاء اللوم على الفيروسات في الأمراض الخطيرة ومن الضروري محاربتها، لكن يجب أن نكون ممتنين للفيروسات لوجود الطبيعة الحية وتنوعها، بما في ذلك وجود البشر.
المؤلف ممتن لزملائه في التعاون العلمي - موظفو معهد شلل الأطفال والتهاب الدماغ الفيروسي الذي سمي على اسمه. M. P. Chumakov RAMS، جامعة موسكو الحكومية. إم في لومونوسوف، معهد البروتين RAS (بوشينو، منطقة موسكو)، جامعة بازل (سويسرا)، جامعة ويسكونسن (الولايات المتحدة الأمريكية)، جامعة نيميغن. رادبودا (هولندا).
يستند المقال إلى محاضرة ألقيت في مدرسة "علم الأحياء الحديث والتكنولوجيات الحيوية للمستقبل" (زفينيجورود، 26 يناير - 1 فبراير 2014).
. بيلوف جي إيه، ليدسكي بي في، ميكيتاس أو في وآخرون. زيادة ثنائية الاتجاه في نفاذية الغلاف النووي عند الإصابة بفيروس شلل الأطفال والتغيرات المصاحبة للمسام النووية // جي فيرول. 2004. ف. 78. ص 10166-10177. دوى:10.1128/JVI.78.18.10166-10177.2004. ليدسكي بي في، هاتو إس، باردينا إم في وآخرون. اضطراب حركة السيتوبلازم النووي الناجم عن فيروسات القلب // جي فيرول. 2006. ف. 80. ص 2705-2717. دوى:10.1128/JVI.80.6.2705-2717.2006
. باردينا إم في، ليدسكي بي في، شيفال إي في وآخرون. إعادة الترتيب الناجم عن فيروس Mengovirus لمجمع المسام النووي: اختطاف آلات الفسفرة الخلوية // جي فيرول. 2009. ف. 83. ص 3150-3161. دوى:10.1128/JVI.01456-08
. ميكيتاس أو في، إيفين واي واي، جوليشيف إس إيه وآخرون. قمع الإصابات الناجمة عن فيروس الحمض النووي الريبي (الفيروس السحائي) وفصلها عن التكاثر الفيروسي عن طريق نزع السلاح المتبادل للخلايا/الفيروسات // جي فيرول. 2012. ف. 86. ص 5574-5583. دوى:10.1128/JVI.07214-11
. Agol V. I.، Belov G. A.، Bienz K. et al. برامج الموت المتنافسة في الخلايا المصابة بفيروس شلل الأطفال: تبديل الالتزام في منتصف الدورة المعدية // جي فيرول. 2000. ف. 74. ص 5534-5541. دوى:10.1128/JVI.74.12.5534-5541.2000
. Agol V. I. تأثيرات الاعتلال الخلوي: مظاهر المناعة الفطرية المعدلة بالفيروس؟ // اتجاهات الميكروبيول. 2012. المجلد 20. ص 570-576. دوى:10.1016/j.tim.2012.09.003
. Koonin E. V., Dolja V. V. منظور مركزي حول تطور الحياة // العملة. رأي. فيرول. 2013. المجلد 3. ص 546-557. دوى:10.1016/j.coviro.2013.06.008
 طبيعة وأصل الفيروسات
طبيعة وأصل الفيروسات بطاقة عمل QR - بطاقة عمل تعتمد على رمز QR، التصميم باستخدام تطبيق ويب
بطاقة عمل QR - بطاقة عمل تعتمد على رمز QR، التصميم باستخدام تطبيق ويب المخطط الفني المضلع للمباني
المخطط الفني المضلع للمباني